Ведущие российские специалисты из Института молекулярной биологии имени В.А. Энгельгардта РАН и Московского государственного университета имени М.В. Ломоносова при грантовой поддержке Российского научного фонда (РНФ) совершили прорыв в понимании тонкого баланса между жизнью и смертью клеток. Гелина Копеина, Анастасия Ефименко и их команда исследовали, каким образом разные виды программируемой гибели клеток влияют на восстановление повреждённых тканей и защиту от опасных заболеваний. Их выводы открывают новые горизонты для медицины будущего, внушая оптимизм для развития терапии травм, хронических и возрастных заболеваний.
Баланс жизни: постоянство обновления и защита от заболеваний
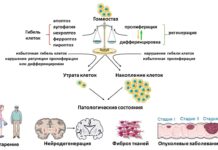
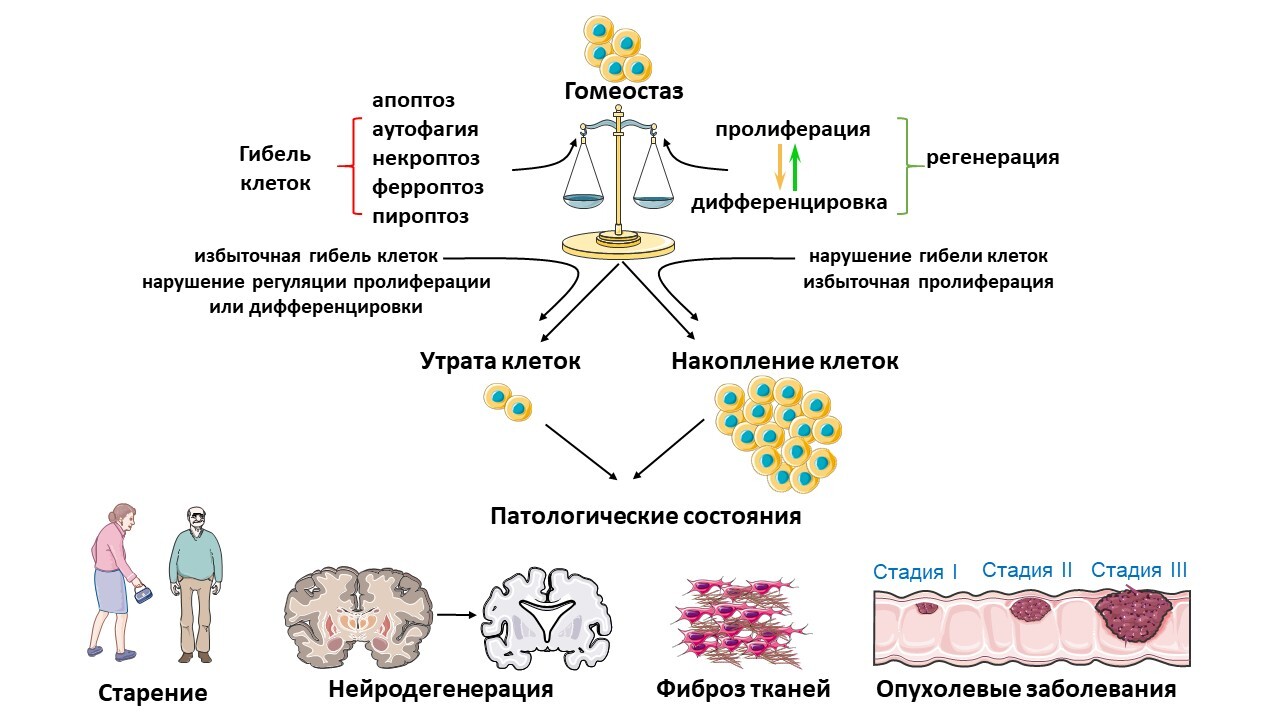
Каждый день в человеческом теле тихо и незаметно завершается жизнь миллионов клеток. Этот процесс — программируемая гибель клеток — чрезвычайно строго регулируется, а нарушения баланса между отмиранием и появлением новых клеток лежат в основе множества опасных болезней, включая рак, фиброз и нейродегенеративные патологии. Поддержание гармонии между делением, специализацией и гибелью клеток — основа устойчивой работы организма. Научившись целенаправленно контролировать эти механизмы, специалисты смогут приближаться к разработке принципиально новых методов лечения целого спектра патологий, включая хронические и возрастные нарушения.
Виды клеточной гибели: апоптоз, некроптоз и ферроптоз под микроскопом
Специалисты из ИМБ имени В.А. Энгельгардта РАН и МГУ рассмотрели более 300 работ по различным типам программируемой гибели клетки — от классического апоптоза до относительно недавно открытых некроптоза и ферроптоза. Научное сообщество описало уже свыше десятка механизмов, благодаря которым клетки завершает свой жизненный цикл. Особый интерес вызывают различия в ходе этих процессов — понимание тонких и зачастую противоположных механизмов открывает путь к точечному вмешательству в патологические процессы.
Апоптоз считается наиболее изученным видом клеточной гибели. Когда клетка умирает по этому сценарию, она распадается на мелкие мембранные структуры — апоптотические тельца, которые быстро захватываются макрофагами иммунной системы. Именно по этой причине апоптоз, в отличие от других форм гибели, не вызывает воспаления в тканях и способствует их благополучному восстановлению.
Контрасты клеточной гибели: от воспаления до регенерации
Совсем иначе происходит некроз, при котором клетка разрушительно разрывается, высвобождая все содержимое и вызывая воспалительный процесс в окружающих тканях. Этот тип гибели нередко ассоциируется с травмами, инфекциями или тяжелыми патологиями, когда воспаление усугубляет общее состояние организма.
Особое внимание учёные уделили ферроптозу — программе клеточной гибели, запускаемой окислительными процессами с участием железа. При ферроптозе происходит повреждение фосфолипидных мембран клеток и накапливаются активные формы кислорода, что приводит к гибели клеток. По словам руководителя исследования Гелины Копеиной, доктор биологических наук и заведующей лабораторией ИМБ имени В.А. Энгельгардта, подобные процессы особенно актуальны при изучении заболеваний сердца, мозга и при старении.
Вклад фундаментальных исследований для медицины будущего
Глубокое изучение механизмов клеточной гибели и их связи с регенерацией тканей открывает широкие перспективы для применения новых терапевтических стратегий в медицине. Исследования Гелины Копеиной, Анастасии Ефименко и их коллег показывают, что управление этими процессами может стать ключом к преодолению тяжелых хронических болезней, травматических повреждений, нарушений обмена веществ и даже возрастных изменений.
Понимание того, когда и как стоит вмешиваться в процессы гибели клеток — например, усиливая апоптоз при борьбе с опухолями или, напротив, тормозя его для ускорения регенерации после травм — позволяет двигаться в сторону развития персонализированной медицины. Поддержка Российского научного фонда (РНФ) способствует формированию научных основ для появления инновационных подходов к лечению самых сложных заболеваний.
Гармония регенерации и обновления: научный взгляд в будущее
Работы учёных из Института молекулярной биологии имени В.А. Энгельгардта РАН и МГУ показывают, что регулирование клеточной гибели лежит в самой основе способности организма к восстановлению. Постоянный обмен клеточных «кадров», своевременное удаление поврежденных и стареющих элементов, быстрая реакция на угрозы — всё это позволяет человеку сохранять здоровье даже в условиях агрессивной внешней среды.
Фундаментальные открытия в области программируемой гибели клеток и регенерации тканей становятся прочным научным фундаментом для будущих технологий долголетия, восстановления органов и борьбы с болезнями, ранее считавшимися необратимыми. Российские исследователи уверенно движутся к тому, чтобы уже в обозримой перспективе изменить представления о возможностях медицины и улучшить качество жизни миллионов людей.
Особенности влияния разных видов гибели клеток
Современные исследования все активнее раскрывают удивительные способности организма к восстановлению, связанные с особенностями гибели клеток. Научные наблюдения показали, что различные пути клеточной смерти по-разному сказываются на процессе заживления тканей. При программируемой гибели клеток — апоптозе — клетки вырабатывают характерные микроскопические пузырьки, называемые везикулами ApoEVs. Они содержат важные биомолекулы — ДНК, РНК, белки и липиды, — и становятся своеобразным «сигналом тревоги» для окружающих здоровых клеток. Этот сигнал активирует рост и деление соседних клеток, способствуя своевременному восполнению утраченных тканей. Благодаря такому обмену организма удается сохранять гармонию между обновлением и удалением клеток. В экспериментальных моделях, например у крыс, препараты на основе ApoEVs показали отличные результаты: скорость заживления ран увеличивалась до 40%.
Воспаление и регенерация — новые взгляды на некроз
Вопреки традиционному представлению, некроз — разновидность гибели клеток, которую часто считают исключительно вредной, — также может выполнять полезную функцию. В момент некроза освобождаются особые сигнальные молекулы DAMPs, которые как «маяки» притягивают макрофаги. Примечательно то, что макрофаги не только убирают остатки погибших клеток, но и «будят» стволовые клетки, побуждая их к восстановлению повреждённых тканей. Исследования на мышах подтвердили: некроз становится важным этапом для полноценного восстановления миелиновой оболочки у нервных клеток головного мозга. Это доказывает, что даже воспалительный процесс способен играть созидательную роль, если происходит под контролем и в нужном контексте.
Обратная сторона медали: активизация опухолевых клеток
Однако столь яркие позитивные эффекты не обходятся без сложностей. Те же сигналы, которые ускоряют восстановление тканей, могут быть использованы и раковыми клетками для собственного роста. Опухолевые клетки зачастую задействуют те же механизмы, что и нормальные, для размножения, а значит, стимулирующее влияние апоптоза и некроза способно привести к быстрому увеличению опухоли или к возникновению рецидивов после лечения. Именно поэтому ученые подчеркивают необходимость дальнейших исследований: одинаковый эффект в разных тканях и для разных типов клеток может нести как пользу, так и риск. Подходы, основанные на модуляции гибели клеток, должны разрабатываться с большой осторожностью и учитывать специфику каждого клинического случая.
Уникальные способности стволовых клеток
В центре внимания исследователей находятся и стволовые клетки — настоящий «золотой запас» регенерации организма. Оказалось, что эти клетки часто обладают высокой устойчивостью к программируемой гибели. Это объясняется их способностью интенсивно вырабатывать защитные белки и восстанавливать поврежденную ДНК, что позволяет сохранить потенциал для обновления тканей даже при повреждениях. Такие свойства обеспечивают организму устойчивый резерв клеток, готовых в любой момент встать на защиту и восстановление своих собратьев. В то же время известны и такие разновидности стволовых клеток, которые реагируют на определённые типы программируемой гибели. Хотя точные механизмы этих процессов изучены пока не до конца, учёные уверены: понимание этого феномена откроет новые горизонты для регенеративной медицины.
Новое будущее для терапии и восстановления
Экспериментальные данные дают вдохновляющую пищу для размышлений: гибель клеток — это не просто этап разрушения, а тонко регулируемый и творческий процесс. В одних ситуациях она активирует регенерацию, в других требует поддержки или корректировки. Чем глубже специалисты познают условия, при которых разные типы гибели клеток включаются и каковы их последствия для организма, тем успешнее становятся поиски революционных методов для лечения травм, возрастных нарушений и разных патологий. Как отмечает руководитель одного из таких проектов, доктор медицинских наук Анастасия Ефименко, центр современных исследований смещается в сторону понимания тонкого баланса между делением и гибелью клеток. В ближайшем будущем ученые планируют более детально исследовать возможности воздействия на эти процессы, чтобы запускать регенерацию тканей целенаправленно и безопасно. Новое поколение экспериментальных моделей уже вовлечено в эти перспективные работы, и результаты обещают открыть новые пути к долгой и здоровой жизни.
Механизмы баланса между гибелью клеток и восстановлением тканей
Современные исследования доказали: здоровое функционирование нашего организма напрямую зависит от тонкого баланса между программируемой гибелью клеток и их обновлением. Именно этот баланс лежит в основе жизнедеятельности, обеспечивая целостность тканей и органов за счет постоянного обновления и устранения поврежденных или устаревших клеток. Благодаря сложным биологическим механизмам, наш организм способен своевременно реагировать на различные негативные воздействия, защищая себя и поддерживая здоровье.
В ходе многочисленных экспериментов учёные установили, что ряд специфических белков и сигнальных путей регулируют процессы апоптоза (естественной гибели клеток) и регенерации. Если этот баланс нарушается, могут возникать различные заболевания — от аутоиммунных реакций до онкологических процессов. Однако новые открытия в области молекулярной биологии позволяют взглянуть оптимистично на будущее, ведь прогресс в науке открывает возможности для эффективной терапии и профилактики подобных нарушений. Понимание основ микроскопических процессов уже сегодня помогает ученым разрабатывать инновационные методики лечения и поддержания общего здоровья.
Перспективы для медицины и здоровья человека
Исследование фундаментальных механизмов взаимодействия между апоптозом и регенерацией может вдохновить на создание принципиально новых медицинских решений. Это даст шанс не просто лечить, а предотвращать развитие многих болезней. Уже сейчас тестируются технологии, позволяющие регулировать клеточные процессы, повышать сопротивляемость организма, а также ускорять восстановление тканей после травм и операций. Всё это внушает уверенность в благоприятных перспективах для продления активной и полноценной жизни.
Источник: indicator.ru