Международный коллектив ученых, включающий специалистов МФТИ, убедительно продемонстрировал потенциал яда паука-кругопряда Argiope lobata для блокирования нейрорецепторов в мозге человека. Эти открытия открывают путь к созданию лекарств против множества нейродегенеративных болезней.
Глутаматные рецепторы и проблема избытка кальция
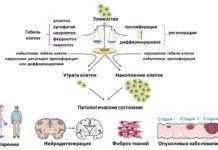
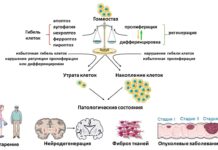
Скоростная передача сигналов между нейронами мозга преимущественно осуществляется через нейромедиаторы. Глутамат, ключевой возбуждающий нейромедиатор, активирует нейроны, связываясь со встроенными в мембрану глутаматными рецепторами. Это открывает ионные каналы для положительных ионов, вызывая деполяризацию и генерацию нервного импульса. Однако при патологиях нервной системы наблюдается чрезмерная активация определенных глутаматных рецепторов, особенно тех, что проводят ионы кальция. Избыточное поступление кальция в нейроны запускает апоптоз, приводя к гибели клеток. Требуются специфические блокаторы для контроля этого процесса.
Структура блокаторов: Природа и синтез
Ученые успешно исследовали молекулярное строение глутаматного рецептора в комплексе с тремя блокаторами. Среди них природный токсин аргиопин из яда Argiope lobata и два искусственных соединения. Все три вещества имеют сходную химическую архитектуру: "голову", похожую на ароматическую аминокислоту, и "хвост" разной длины с аминогруппами, соединенными углеводородными цепями. Анализ проводился методом криоэлектронной микроскопии, отмеченным Нобелевской премией в 2017 году.
Механизм блокировки: Как действует яд
"Мы обнаружили, что блокаторы проникают внутрь рецептора при его активации глутаматом", поясняет руководитель исследования Александр Соболевский, выпускник МФТИ и завлаб Колумбийского университета (Нью-Йорк, США). "Их положительно заряженный хвост фиксируется в узкой отрицательно заряженной зоне ионного канала селективном фильтре, пропускающем катионы. Пройти дальше мешает голова молекулы, застревающая во внутренней полости рецептора".
Перспективы для лечения тяжелых заболеваний
"Эти данные критически важны для разработки селективных блокаторов кальций-проницаемых глутаматных рецепторов ключевой фармакологической мишени", рассказывает Мария Елшанская, выпускница МФТИ и научный сотрудник Колумбийского университета. "Они необходимы для терапии бокового амиотрофического склероза, эпилепсии, ишемических повреждений нейронов, а также нейродегенерации при болезнях Альцгеймера и Паркинсона".
От токсина к лекарству: История открытия
"Интересно, что в основе работы токсин паука, открытый академиком Евгением Гришиным еще в 1986 году", добавляет Александр Василевский, преподаватель МФТИ и завлалаб в ИБХ РАН. "Вещества, используемые пауком для поражения жертвы, теперь служат нам для изучения нервной системы и создания лекарств против нейродегенераций".
Селективность ключ к безопасности
Ключевое преимущество природных токсинов и их синтетических аналогов их избирательность. Они блокируют только "проблемные" кальций-проницаемые рецепторы, не затрагивая жизненно важные рецепторы, непроницаемые для кальция и ответственные за нормальную передачу нервных импульсов. Будущие препараты на их основе будут воздействовать исключительно на патологические мишени.
Будущее терапии: Спасение нейронов
Теперь, когда детально изучен механизм связывания токсинов в канале рецептора, химики смогут проектировать новые, высокоэффективные блокаторы. Эти соединения предотвратят опасное проникновение избытка кальция в нейроны при заболеваниях нервной системы. Это спасет нервные клетки от гибели и восстановит здоровое функционирование нервной системы.
Источник: scientificrussia.ru