Генетическое сходство человека и шимпанзе превышает 98%, несмотря на это, частота развития онкологических заболеваний у людей существенно выше, чем у наших ближайших эволюционных родственников. Это удивительное наблюдение указывает на наличие тонких, но критически важных различий в генах, которые могли возникнуть в ходе эволюции человека. Понимание этих особенностей способно раскрыть фундаментальные причины уязвимости к раку и помочь создать более эффективные методы его профилактики и лечения.
Иммунотерапия: новые горизонты в противораковой борьбе
Современная онкология делает ставку на иммунотерапию — подход, при котором иммунная система самого пациента привлекается для атаки на злокачественные клетки. Наиболее заметный успех был достигнут в терапии CAR-T клетками: генетически модифицированные Т-лимфоциты способны находить и уничтожать опухолевые клетки, проявляя невероятную эффективность в лечении гематологических разновидностей рака.
Тем не менее, в случае солидных опухолей — таких, как рак молочной железы, кишечника или легкого — эффективность иммунотерапии до сих пор ограничена. Дело в том, что плотное опухолевое микроокружение создает дополнительные преграды для проникновения и работы иммунных клеток. Разгадка природы этих барьеров может открыть путь к созданию действительно универсальных подходов к лечению всех разновидностей рака.
Fas-лиганд: ключевой элемент иммунитета против опухолей
В центре механизма противоопухолевого иммунитета стоит белок, известный как Fas-лиганд (FasL). Этот белок экспрессируется на поверхности активированных Т-киллеров — главных «солдат» иммунной системы. В момент, когда Т-киллер сталкивается с опухолевой клеткой, Fas-лиганд взаимодействует с рецептором Fas, запуская в мишени цепь событий, приводящих к апоптозу, то есть к «программируемому саморазрушению» раковых клеток.
FasL — это, по сути, основное «оружие» иммунной системы в борьбе с раком. Однако в тканях солидных опухолей действие этого «оружия» неоднократно оказывается заблокированным, и до сих пор причины этого феномена оставались не до конца выявленными.
Мутация в Fas-лиганде: история одной замены, изменившей судьбу человека
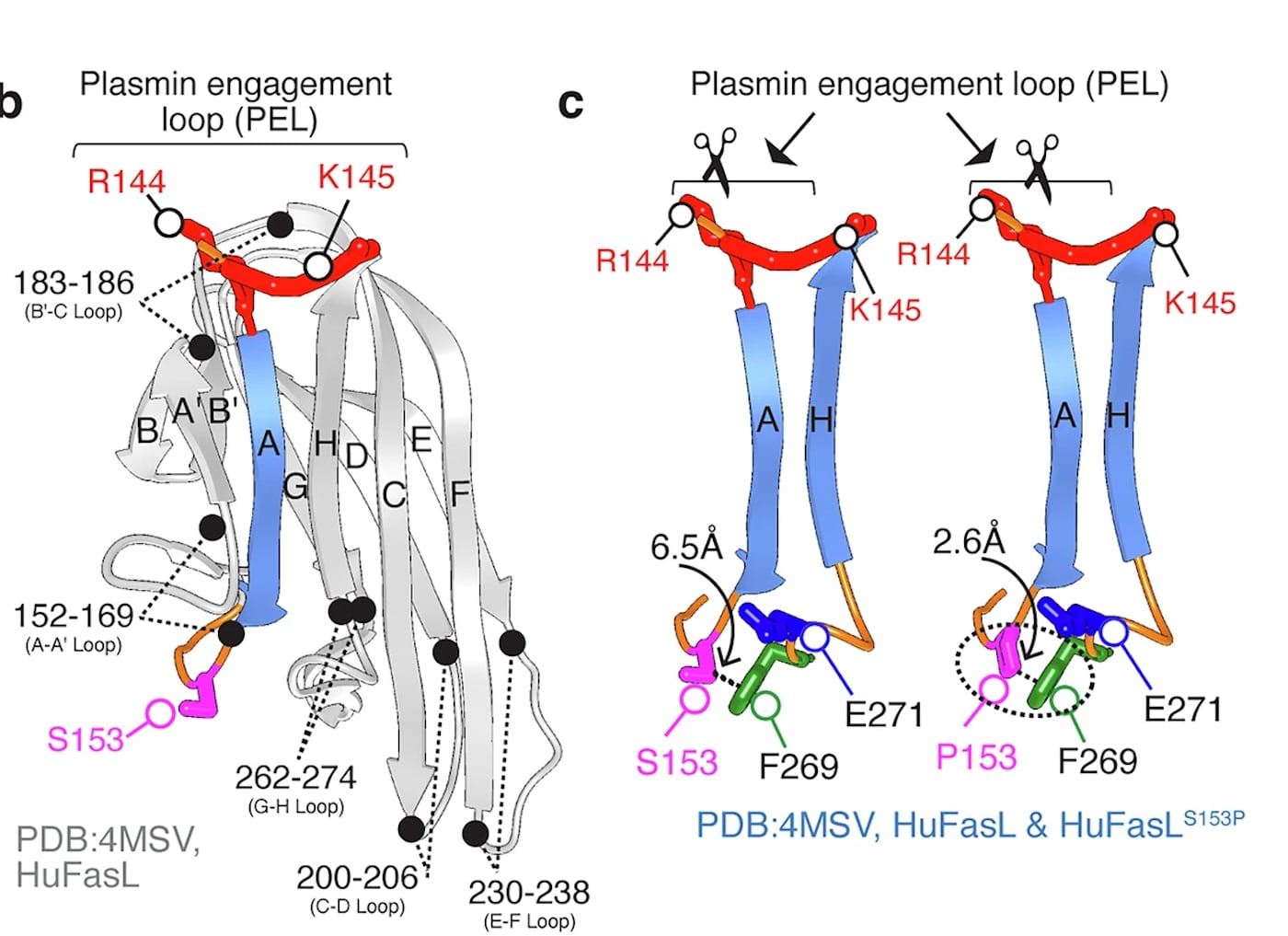
Недавно проведенные исследования позволили обнаружить всего одно значимое отличие в белке FasL у человека и других приматов. Разница заключается в 153-й позиции аминокислотной цепи: у человека этот участок занимает аминокислота серин, а у других приматов — пролин. На первый взгляд, столь незначительная разница привела к серьезнейшим функциональным последствиям. Выяснилось, что именно серин делает человеческий Fas-лиганд крайне чувствительным к действию особого фермента — плазмина.
Плазмин — это протеаза (фермент, расщепляющий белки), которая активно секретируется многими агрессивными опухолями. Плазмин помогает раку разрушать ткани и распространяться по организму. Когда плазмин встречает Fas-лиганд с серином в 153-й позиции, он легко разрезает белковую цепь, полностью деактивируя FasL. В то же время Fas-лиганд с пролином является устойчивым к действию плазмина, так как пролин стабилизирует белковую структуру и защищает ее от разрушения.
Для проверки этих гипотез были созданы искусственные (рекомбинантные) варианты Fas-лиганда: обычный человеческий вариант, вариант макаки-резуса, а также две гибридные формы, где аминокислота в ключевой позиции была заменена на противоположную. Результаты показали: только цепь с серином подвергается разрушению плазмином, а с пролином сохраняет свою функцию, невзирая на присутствие фермента.
Плазмин как новая цель для усовершенствования иммунотерапии
Даннное открытие подталкивает к прямому и эффективному способу обходить защитные механизмы опухоли. Ученые опробовали два метода: применение ингибитора плазмина (апротинина) и создание особых антител, которые прикрывают участок, восприимчивый к ферменту, не давая плазмину возможности разрушить Fas-лиганд. Оба способа показали высокую эффективность: FasL вновь оказывался способным индуцировать гибель раковых клеток даже в агрессивной опухолевой среде, богатой плазмином.
Таким образом, появилось реальное направление для разработки новых комбинаций иммунотерапевтических препаратов: объединение уже существующих методов с блокаторами плазмина способно значительно повысить эффективность борьбы с солидными опухолями, делая иммунотерапию гораздо более универсальной. Это открывает перед пациентами дополнительные перспективы и укрепляет веру в победу над раком.
Эволюционный компромисс: интеллект в обмен на устойчивость к раку?
Эти исследования не только несут практическую пользу для онкологии, но и проливают свет на сложную эволюционную историю человека. Мутация, которая ослабила функцию Fas-лиганда и повысила восприимчивость к онкологическим заболеваниям, могла одновременно оказаться выгодной в другом аспекте. Есть основания полагать, что снижение активности FasL способствовало увеличению размеров человеческого мозга по сравнению с близкими родственниками.
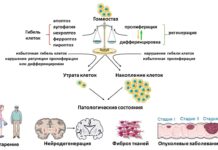
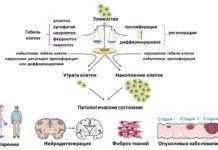
Fas-лиганд играет роль в регуляции апоптоза не только в иммунитете, но и на этапах эмбрионального развития, в частности, формировании нервной системы. Ограниченная активность FasL могла привести к тому, что у предков человека отмирало меньше нейрональных клеток-предшественников, что обеспечило быстрый рост и мощное развитие коры головного мозга. Это классический пример так называемой антагонистической плейотропии — когда одно генетическое изменение полезно для одних функций организма, но повышает риск развития других патологий, в данном случае опухолей.
Светлое будущее: новые стратегии лечения и оптимизма для пациентов
Открытие роли мутации Fas-лиганда и его взаимодействия с плазмином не только обогащает наши знания о механизмах развития рака, но и дает надежду миллионам пациентов. Уже в обозримом будущем возможны комбинации иммунотерапии с блокаторами плазмина, что сделает лечение солидных опухолей гораздо эффективнее и доступнее.
Понимание тонких эволюционных механизмов меняет представления о природе рака и подсказывает, как побеждать болезнь. Подобные исследования внушают оптимизм, ведь благодаря им мы становимся ближе к миру, где рак можно будет не только контролировать, но и полностью излечивать. Наука продолжает делать шаги, которые делают этот день всё ближе.
Источник: naked-science.ru